









 Рейтинг: 4.0/5.0 (1893 проголосовавших)
Рейтинг: 4.0/5.0 (1893 проголосовавших)Категория: Инструкции
Виталина » 27 фев 2014, 11:27
«__»________ г №_______
О назначении уполномоченного по качеству
На основании Приказа Минздрава РФ от 12 февраля 2007г. N 110 "О порядке назначения и выписывания лекарственных средств, изделий медицинского назначения и специализированных продуктов лечебного питания" и Приказа Министерства здравоохранения и социального развития РФ от 4 марта 20036 г. N80 "Об утверждении отраслевого стандарта «Правила отпуска (реализации) лекарственных средств в аптечных организациях. Основные положения».
1. Назначить уполномоченного по качеству в каждом аптечном учреждении:
- в аптечном учреждении №1 ЗАУ Иванову Марию Ивановну
2. Контроль за выполнением приказа возложить на директора…
Но если ОСТ 80 будет отменен, то смысл в этом приказе?
П Р И К А З № 5
о назначении уполномоченного по качеству
Приказываю:
1. Назначить уполномоченным по качеству заведующую аптекой.
2. Ответственный по качеству. в своей деятельности руководствуется Положением об уполномоченном по качеству (приложение №1)
3. Возложить обязанности отслеживать забракованные препараты с применением всемирной сети Интернет – уполномоченного по качеству провизора -.
4. Организовать отслеживание забракованных препаратов с периодичностью 1 раз в день, 5 рабочих дней в неделю.
5. Контроль за исполнением данного приказа возложить на Генерального директора Общества –.
Генеральный директор.
С Приказом ознакомлены:
[число, месяц, год]
Должностная инструкция уполномоченного по качеству [наименование организации]
Настоящая должностная инструкция разработана и утверждена в соответствии с положениями Трудового кодекса Российской Федерации. "Правилами отпуска (реализации) лекарственных средств в аптечных организациях", утвержденными приказом Министерства здравоохранения Российской Федерации N 80 от 04.03.2003 г. и иных нормативно-правовых актов, регулирующих трудовые правоотношения.
1. Общие положения1.1. Уполномоченный по качеству относится к категории руководителей и непосредственно подчиняется руководителю [наименование организации].
1.2. Уполномоченный по качеству назначается на должность и освобождается от нее приказом руководителя [наименование организации].
1.3. На должность уполномоченного по качеству назначается лицо, имеющее высшее или среднее фармацевтическое образование, сертификат специалиста и стаж работы по специальности не менее трех лет.
1.4. На время отсутствия уполномоченного по качеству его должностные обязанности выполняет руководитель [наименование организации].
1.5. Уполномоченный по качеству должен знать:
- нормативные документы Министерства здравоохранения Российской Федерации;
- методические, нормативные и другие материалы по контролю качества лекарственных средств;
- приказы, указания руководителя организации;
- положения и инструкции по защите прав потребителей;
- порядок оформления и организации документооборота;
- правила и нормы охраны труда, техники безопасности, производственной санитарии и противопожарной безопасности.
2. Должностные обязанностиНа уполномоченного по качеству возлагаются следующие должностные обязанности:
2.1. Обеспечение анализа и систематизации поступающей в аптечную организацию документации и информации по качеству лекарственных средств, а также сведений о забракованных и фальсифицированных лекарственных средствах.
2.2. Доведение полученной информации до сведения руководителя аптеки и руководителей структурных подразделений.
2.3. Осуществление контроля за организацией приемки, хранения, изготовления и отпуска лекарственных средств в соответствии с действующими требованиями осуществления фармацевтической деятельности.
2.4. Проведение внутренних проверок на соответствие аптечной организации требованиям ОСТа 91500.05.0007-2003 "Правила отпуска (реализации) лекарственных средств в аптечных организациях. Основные положения".
2.5. При наличии некачественной лекарственной продукции принятие срочных мер к возврату поставщику либо уничтожению.
2.6. Разработка необходимых инструкций, касающихся вопросов обеспечения качества.
2.7. Ведение необходимой документации.
2.8. Соблюдение правил личной гигиены, включая использование специальной одежды.
2.9. Учет недоброкачественных и фальсифицированных лекарственных средств.
2.10. [Другие должностные обязанности].
3. ПраваУполномоченный по качеству имеет право:
3.1. На все предусмотренные законодательством Российской Федерации социальные гарантии.
3.2. Получать от руководства организации в установленном порядке информацию, которая необходима для выполнения возложенных на него задач.
3.3. Предъявлять претензии к качеству товара поставщикам.
3.4. Привлекать соответствующих специалистов для проведения контроля, а также использовать в работе необходимые технические средства.
3.5. Действовать от имени организации во взаимоотношениях с организациями-поставщиками, органами по сертификации, контролирующими органами.
3.6. Знакомиться с проектами приказов руководства, касающимися его деятельности.
3.7. Повышать свою профессиональную квалификацию.
3.8. Вносить предложения руководству по улучшению организации и условий своего труда.
3.9. Другие права, предусмотренные трудовым законодательством Российской Федерации.
4. ОтветственностьУполномоченный по качеству несет ответственность:
4.1. За неисполнение, ненадлежащее исполнение обязанностей, предусмотренных настоящей инструкцией, - в пределах, определенных трудовым законодательством Российской Федерации.
4.2. За совершенные в процессе осуществления своей деятельности правонарушения - в пределах, определенных действующим административным, уголовным и гражданским законодательством Российской Федерации.
4.3. За причинение материального ущерба работодателю - в пределах, определенных действующим трудовым и гражданским законодательством Российской Федерации.
Должностная инструкция разработана в соответствии с [наименование, номер и дата документа].
Руководитель кадровой службы
[число, месяц, год]
[число, месяц, год]
Руководителям аптечных учреждений
В целях обеспечения безопасности лекарственной продукции, реализуемой на территории Воронежской области и организации действенного контроля качества лекарственных средств в медицинских и фармацевтических организациях, направляем вам типовую форму должностной инструкции уполномоченного по качеству лекарственных средств (приложение).
В этой связи, для создания единого подхода при организации работы специалиста уполномоченного по качеству лекарственных средств и предотвращения реализации некачественной лекарственной продукции в ваших подведомственных организациях, необходимо пересмотреть имеющуюся инструкцию и взять за основу вышеуказанную должностную инструкцию.
С учетом периода заключения договоров с ГУЗ «Воронежский ЦКК и СЛС», обращаем особое внимание на содержание предоставляемого пакета документов (в частности - должностной инструкции уполномоченного по качеству лекарственных средств).
Обновленную и утвержденную инструкцию предоставить в ГУЗ «Воронежский ЦКК и СЛС».
ГУЗ «Воронежский ЦКК и СЛС» О. А. Селютин
Должностная инструкция уполномоченного по качеству в сфере обращения лекарственных средств
На должность уполномоченного по качеству назначается лицо с высшим или средним фармацевтическим образованием, имеющее сертификат специалиста и стаж работы по специальности не менее 3 лет.*
Основной задачей уполномоченного по качеству является обеспечение качества лекарственных средств в соответствии с требованиями действующих нормативных документов.
Уполномоченный по качеству назначается на должность и освобождается от нее приказом руководителя учреждения в установленном трудовым законодательством порядке.
Уполномоченный по качеству руководствуется в своей работе действующим законодательством Российской Федерации в сфере здравоохранения, нормативно-правовыми актами, методическими и другими материалами Министерства здравоохранения и социального развития Российской Федерации, Федеральной службы по надзору в сфере здравоохранения и социального развития, органов государственной власти Воронежской области, приказами, указаниями руководителя организации и настоящей инструкцией.
Уполномоченный по качеству обязан:
Руководящие документы Минздравсоцразвития РФ и Ростехрегулирования РФ, Федеральной службы по надзору в сфере здравоохранения и социального развития, территориального управления Росздравнадзора, нормативно-правовые акты Воронежской области, департамента здравоохранения Воронежской области, нормативные документы ГУЗ "Воронежский ЦККиСЛС", относящиеся к вопросам организации контроля качества лекарственных средств;
Профиль, структуру, специализацию и особенности работы организации;
Положения и инструкции по Защите прав потребителя;
Правила сертификации/декларирования лекарственных средств;
Порядок оформления и организации документооборота;
Правила и нормы охраны труда, техники безопасности, производственной санитарии и противопожарной безопасности.
- проведение предупредительных мероприятий с целью недопущения оборота фальсифицированных и недоброкачественных лекарственных средств в соответствии с приказом департамента здравоохранения и социального развития Воронежской области от 02.03.2009г. №476/ОД «Об утверждении Положения о порядке проведения мероприятий, направленных на предотвращение поступления фальсифицированных и недоброкачественных лекарственных средств на территорию Воронежской области», приказом ГУЗ «Воронежский ЦКК и СЛС» от 18.03.2009 г. № 27 « Об утверждении Методических указаний по порядку проведения контроля качества фармацевтических субстанций и вспомогательных веществ». и письмом ГУЗ «Воронежский ЦККиСЛС» от 09.11.2009г.;
проведение приемочного контроля, включающего проверку лекарственных средств по показателям "Описание", "Упаковка", "Маркировка";
проверку документов по качеству (сертификаты/декларации соответствия), приложения к товаро-сопроводительным документам, содержащие информацию о сертификате/декларации соответствия;
направление лекарственных средств для проведения испытаний в ГУЗ «Воронежский ЦККиСЛС» в случае сомнения в их качестве;
контроль за отсутствием недоброкачественных и фальсифицированных лекарственных средств с использованием ИПП «Контроль-Фальсификат» ГУЗ «Воронежский ЦККиСЛС» (не реже 2-х раз в день);
принятие незамедлительных мер при наличии некачественной лекарственной продукции, к возврату поставщику, либо уничтожению;
уведомление (в течении 24 часов) ГУЗ «Воронежский ЦККиСЛС» о наличии недоброкачественных/фальсифицированных лекарственных средств;
представление оперативной и ежемесячной отчетности в ГУЗ «Воронежский ЦККиСЛС» о недоброкачественных/фальсифицированных лекарственных средств;
учет недоброкачественных и фальсифицированных лекарственных средств;
контроль за соблюдением сроков годности лекарственных средств;
контроль за соблюдением уровней «холодовой цепи» медицинских иммунобиологических препаратов;
контроль за соблюдением правил хранения лекарственных средств, санитарного режима, согласно требований действующих нормативно-правовых актов;
проведение самоинспекции (внутренних проверок) на соответствие требованиям Отраслевых стандартов;
- организацию мероприятий при проведении целевого мониторинга недоброкачественных и фальсифицированных лекарственных средств в организации/учреждении;
- совершенствование системы менеджмента качества организации/учреждения;
контроль за выполнением правил внутреннего трудового распорядка, действующего в организации;
ведение необходимой документации.
Уполномоченный по качеству имеет право:
получать от руководства организации в установленном порядке информацию, которая необходима для выполнения возложенных на него задач;
пользоваться материальными ценностями организации/учреждения (множительная, компьютерная и оргтехника, автотранспорт), а также всеми документами, необходимыми для выполнения возложенных на него обязанностей;
предъявлять претензии к качеству товара поставщикам;
действовать от имени организации во взаимоотношениях с организациями-поставщиками, органами по сертификации, контролирующими органами;
вносить предложения руководству по улучшению организации и условий своего труда.
Уполномоченный по качеству непосредственно подчиняется руководителю организации или лицу его замещающему.
Уполномоченный по качеству несет персональную ответственность за:
несвоевременное и нечеткое, выполнение функциональных обязанностей в соответствии с действующим законодательством;
допуск к реализации недоброкачественной, фальсифицированной лекарственной продукции;
несвоевременное изъятие из обращения недоброкачественной, фальсифицированной лекарственной продукции;
невыполнение письменных и устных распоряжений руководства организации;
правильное и своевременное ведение установленных документов учета и отчетности;
санитарное состояние своего рабочего места.
С инструкцией ознакомлен
* В случае отсутствия специалиста соответствующей квалификации, указанной в п.1, раздела I, допускается назначение другого должностного лица при согласовании.

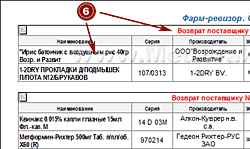 Оформление возврата поставщику товара из аптеки.
Оформление возврата поставщику товара из аптеки.
 Скидки при реализации лекарств. Настройка скидки с подтверждением при продаже. Настройка скидок по времени.
Скидки при реализации лекарств. Настройка скидки с подтверждением при продаже. Настройка скидок по времени.
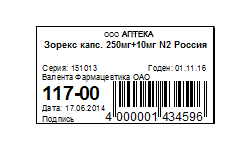 Печать этикеток со штрих-кодом на обычный принтер и принтер штрих-кодов. Печать штрих-кодов по количеству товара.
Печать этикеток со штрих-кодом на обычный принтер и принтер штрих-кодов. Печать штрих-кодов по количеству товара.
 Обзор новых нормативных документов в области здравоохранения, вступивших в силу с января 2016 года.
Обзор новых нормативных документов в области здравоохранения, вступивших в силу с января 2016 года.
 Новая система индивидуальной маркировки и мониторинга движения лекарственных препаратов.
Новая система индивидуальной маркировки и мониторинга движения лекарственных препаратов.
 Противоречия в законодательстве при ценообразовании на ЖНВЛП.
Противоречия в законодательстве при ценообразовании на ЖНВЛП.
 Расчет розничных цен на жизненно важные лекарственные средства. Формирование отпускной цены ЖНВЛП.
Расчет розничных цен на жизненно важные лекарственные средства. Формирование отпускной цены ЖНВЛП.
 Брак, опасный для жизни. Какие лекарства чаще всего подделывают или продают бракованными.
Брак, опасный для жизни. Какие лекарства чаще всего подделывают или продают бракованными.
 Подделки ценою в жизнь. Ответственность за некачественные лекарственные препараты.
Подделки ценою в жизнь. Ответственность за некачественные лекарственные препараты.
 Контроль качества лекарственных средств, поступивших в Воронежскую область в 2015 году.
Контроль качества лекарственных средств, поступивших в Воронежскую область в 2015 году.
 Обновленный перечень нормативных документов, регламентирующих организацию контроля качества лекарственных средств.
Обновленный перечень нормативных документов, регламентирующих организацию контроля качества лекарственных средств.
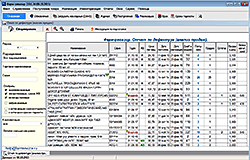 Отчёт по дефектуре. Анализ продаж в аптеке. Расчет срока, на который хватит оставшегося товара.
Отчёт по дефектуре. Анализ продаж в аптеке. Расчет срока, на который хватит оставшегося товара.
 Подготовка отчета по дистанционному мониторингу лекарственных средств для центра контроля качества.
Горячая линия
Подготовка отчета по дистанционному мониторингу лекарственных средств для центра контроля качества.
Горячая линия

для приема обращений по вопросам качества лекарственных средств:
8-800-775-36-03

База данных забракованных медицинских средств. Перечень обновляется ежедневно, содержит ссылки на нормативные документы, согласно которым препарат признан фальсификатом. В настоящий момент в базе около 25 000 лекарственных препаратов.
Нормативные документы.
Тексты нормативных документов, регулирующие фармацевтическую, медицинскую деятельность и контроль качества лекарственных средств. Новые документы подключаются 3-4 раза в неделю. В настоящий момент в базе более 16 000 нормативных документов.
ЦЕНТР КОНТРОЛЯ КАЧЕСТВА
Воронежский центр контроля качества и сертификации лекарственных средств был создан для предотвращения оборота фальсифицированных и недоброкачественных лекарственных средств. Центр непосредственно работает под руководством Департамента здравоохранения Воронежской области и в тесном взаимодействии с Федеральным и территориальным управлением Росздравнадзора, Роспотребнадзора, Прокуратурой и правоохранительными органами Воронежской области. В составе Центра функционируют отдел контроля качества (испытательная лаборатория), отдел фармацевтической информации и отдел сертификации и инспекционного контроля.
Фармацевтика и медицина. Статьи и публикации.
В этом разделе можно ознакомиться с информацией по следующей тематике: Производители фармацевтической продукции. Фальсификаты. Подделка лекарственных препаратов.
Внимание! При пользовании статьями, консультациями и комментариями просим Вас обращать внимание на дату написания материала
Вопрос:
Правомерно ли требование лицензирующего органа о наличии удостоверения у уполномоченного по качеству о краткосрочном повышении квалификации «Организация приемочного контроля в условиях аптеки»? В аптечной сети может быть один уполномоченный по качеству или в каждой аптеке (аптечном пункте) должен быть свой, аптеки занимаются самостоятельным (не централизованным) закупом?
Должность уполномоченного по качеству введена в аптечных организациях пунктом 9.9 Отраслевого стандарта «Правила отпуска (реализации) лекарственных средств в аптечных организациях. Основные положения» ОСТ 91500.05.0007-2003, утвержденного Приказом Минздрава РФ от 04.03.2003 г. N 80 (в ред. 18.04.2007 г.), согласно которому руководитель аптечной организации назначает из руководящего персонала уполномоченного по качеству.
Из формулировки указанного пункта Стандарта однозначно вытекает, что уполномоченный по качеству назначается один на всю аптечную организацию независимо от количества у организации обособленных подразделений.
Никаких иных сведений или разъяснений о функциональных обязанностях такого сотрудника, требованиях к его образованию или опыту работы, характере его взаимоотношений с другими сотрудниками фармацевтической организации и т.п. нет ни в одном официальном документе - ни в нормативном правовом акте, ни в каких-либо разъяснительных или правоприменительных документах.
Таким образом, деятельность уполномоченного по качеству аптечной организации действующим законодательством практически никак не регламентирована.
Следовательно, требование лицензирующего органа о наличии у уполномоченного по качеству указанного в тексте вопроса удостоверения ничем не обосновано.
Директор юридической
компании «Юнико-94»
М.И. Милушин
ПО КАЧЕСТВУ УПОЛНОМОЧЕН
В настоящей статье хотелось бы продолжить начатую в N 11 тему уполномоченного по качеству, и его значение в аптечной организации. Новизна этого правового института вызывает множество вопросов, как у участников фармацевтического рынка, так и у представителей судебного аппарата, правоохранительных органов и т.д. в связи с чем тема остается крайне актуальной.
Стоит напомнить, что в соответствии с ОСТом 91500.05.0007-2003 "Правила отпуска (реализации) лекарственных средств в аптечных организациях. Основные положения", утвержденным приказом Министерства здравоохранения Российской Федерации от 4 марта 2003 г. N 80, уполномоченный по качеству отвечает за фармацевтическую деятельность, то есть нормированную п. 4 постановления Правительства Российской Федерации от 6 июля 2006 г. N 416 "Об утверждении Положения о лицензировании фармацевтической деятельности".
В соответствии с этим пунктом требованиями, относимыми к ведению уполномоченного по качеству, являются:
1). документация на объект такого рода, как правоустанавливающие документы на недвижимость заключения санитарной службы, а также документы на оборудование объекта;
2). требования для деятельности, связанной соответственно с розничной либо оптовой торговлей лекарственными средствами, а также с производством лекарств;
3). требования, касающиеся так называемых проблемных лекарственных средств, то есть лекарств с истекшим сроком годности, фальсификатами и т.д.;
4). документация на персонал объекта - документы об образовании и трудовые договоры.
В связи с этим систематизация осуществляемого контроля уполномоченным по качеству является важнейшим требованием к его должностным обязанностям.
В соответствии с п. 9.3. ОСТа 91500.05.0007-2003 "Правила отпуска (реализации) лекарственных средств в аптечных организациях. Основные положения" ". аптечной организацией должны регулярно проводиться внутренние проверки на соответствие требованиям настоящего ОСТа". Таким образом, уполномоченным по качеству периодически должны проводиться так называемые внутренние мероприятия по контролю работы организации. Объем работ охватывается таким значительным правовым актом, как ОСТ 91500.05.0007-2003, который можно разделить на вышеприведенные 4 типа требований постановления N 416. То есть проводимые контрольные мероприятия, а соответственно, и учетную документацию к ним, можно также делить на указанные области.
1. Документация на объект включает в себя, прежде всего, правоустанавливающие документы, как то: договор аренды, свидетельство о праве собственности на имущество, акт приема-передачи и т.д. А также "смежные" документы - заключения санитарно-эпидемиологической и противопожарной служб.
Документация на оборудование подразумевает также правоустанавливающие документы на имущество - к примеру, документы приобретения холодильных камер, шкафов, акты гарантийного обслуживания и т.д.
Указанные документы должны быть особо упорядочены, копии с них должны храниться под рукой на случай проверки. И, конечно, должна вестись работа по восполнению всех недостающих документов.
2. Контроль за работой с лекарственными средствами - самый многоплановый вид деятельности уполномоченного по качеству. Помимо курирования расположения лекарственных средств их требованиям (термолабильные, чувствительные к свету и т.д.), местонахождения-выкладки (на витрине, в шкафах списков), следует также выяснять организацию процедур приемки лекарственных средств, хранения и отпуска. Помимо этого, не стоит забывать о таких документах, как журналы учета показаний приборов, регистрирующих параметры воздуха, журнал учета отпуска препаратов, подлежащих предметно-количественному учету, и т.д. в зависимости от перечня оказываемых организацией услуг.
3. Работа с "проблемными" лекарственными средствами, как правило, большей частью возложена на компьютерные программы, обновляющие базы фальсификатов, останавливающие отпуск товара в случае истечения срока годности и т.д. Однако следует проверять работоспособность этой системы в организации, налажена ли процедура возврата поставщикам и уничтожения товара.
4. Документация на персонал подразумевает курирование наличия всех дипломов специалистов, сертификатов, трудовых договоров, приказов о назначении на должность, должностных инструкций и прочих "кадровых" бумаг.
Уполномоченный по качеству должен обеспечить хранение всей указанной документации или хотя бы копий всех документов в удобном месте, чтобы была возможность оперативно представить по требованию проверяющих любую нужную информацию. Все показатели и характеристики обозначенных типовых "объектов" внутренних проверок должны быть отражены в соответствующем журнале. Для каждой организации следует индивидуально составлять такой учетный журнал, который должным образом, кроме систематизации надзорных функций уполномоченного по качеству, будет удостоверять надлежащую добросовестность лицензиата даже в случае выявления каких-либо нарушений.
Юрисконсульт ФГУ КМЦЛ
Подписано в печать
Ассоциация содействует в оказании услуги в продаже лесоматериалов: лес доска брус по выгодным ценам на постоянной основе. Лесопродукция отличного качества.
Качество — это один из основных критериев оценки продукции, которым руководствуется потребитель в принятии решений по приобретению того или иного товара. Качество лекарственных средств — это особенно важный показатель, т.к. в отношении выбора лекарственных средств пациент не свободен – лекарство ему назначает врач. Отсюда вывод: любое лекарство должно обладать высоким качеством, поскольку оно непосредственно влияет на здоровье и жизнь человека.
Сычева Вера Николаевна
Зам. директора ГУЗ «Нижегородский областной центр по контролю качества и сертификации лекарственных средств»
Главенствующая роль в системе государственного контроля, направленного на обеспечение качества лекарственных средств, находящихся в обращении, принадлежит Росздравнадзору и его территориальным управлениям.
Государственный контроль охватывает все этапы жизненного цикла лекарственного средства, начиная от разработки, внедрения на рынок и заканчивая уничтожением.
Сегодня государство предъявляет серьезные требования к разработчикам и производителям лекарственных средств по вопросам качества, эффективности и безопасности.
Однако важно не только разработать и произвести высококачественный и эффективный препарат, но и сохранить его на всех этапах движения от производителя до потребителя, сведя к минимуму любой риск для его качества. И эта задача лежит на секторах оптовой и розничной продажи.
Лекарственные средства (ЛС) — продукция, подлежащая обязательному подтверждению соответствия в форме декларирования соответствия, и вся лекарственная продукция реализуется только при наличии документа, подтверждающего качество. Однако неоспоримым фактом является то, что на пути от производителя до потребителя лекарства проходят цепь дистрибуции, и на каждом этапе своего движения в результате нарушений условий хранения и транспортировки лекарственные средства (даже имеющие декларацию о соответствии) могут утратить свои качественные показатели.
В целях сохранения качества реализуемой продукции на предприятиях оптовой торговли и в розничной аптечной сети должны быть разработаны и внедрены системы обеспечения качества.
Аптечная организация несет особую ответственность за реализуемый ею товар, т.к. является конечным пунктом на пути движения лекарства к потребителю, и в этой связи аптечному предприятию важно создать эффективную систему управления качеством ЛС от их поступления в аптеку до реализации населению, и обеспечивающую покупателям приобретение доброкачественной медицинской продукции.
В соответствии с главой IX «Обеспечение качества лекарственных препаратов (лекарственных средств) в аптечных организациях» приказа Минздрава РФ от 04.03.03 №80 (ред. от 18.04.07) «Об утверждении Отраслевого стандарта «Правила отпуска (реализации) лекарственных средств в аптечных организациях. Основные Положения» (вместе с ОСТ 91500.05.0007-2003)» в аптечной организации должна быть сформирована система управления качеством аптечной организации. По сути, это не что иное, как система менеджмента качества (СМК).
Какие стандарты качества нужно взять за основу, что такое СМК, каковы ее принципы, как разработать СМК на предприятии, с чего начать, как организовать работу в соответствии с этой системой подробно рассматривалось на страницах специализированных изданий.
Разработка СМК — достаточно сложный, кропотливый процесс, требующий временных затрат и кадровых ресурсов.
Прежде всего, необходимо обучить на специализированных курсах тех специалистов, которым будет поручена разработка и внедрение на предприятии системы менеджмента качества.
Следует определить основные процессы, установить последовательность и взаимодействие этих процессов; определить критерии и методы обеспечения результативной работы и управления этими процессами; обеспечить наличие ресурсов и информации, необходимой для поддержания работы и наблюдения за этими процессами; организовать наблюдение, оценку и анализ процессов; обеспечить внутренний аудит, анализ со стороны руководства, управление несоответствующей продукцией, проведение корректирующих и предупреждающих действий; установить ответственность за исполнение процессов в должностных инструкциях, документированных процедурах.
Необходимо разработать политику и цели в области качества, руководство по качеству, документированные процедуры; подготовить инструкции (по технике безопасности, должностные, рабочие), внешнюю нормативную документацию (Стандарты, ТУ, Регламенты и др.), положения о подразделениях, техническую документацию по видам деятельности, организационно-распорядительную документацию, записи о качестве.
Часто руководители аптечных предприятий при разработке СМК обращаются за помощью к консультантам, а это предполагает затрату денежных средств.
К сожалению, в большинстве аптек сегодня отсутствует система управления качеством, хотя уполномоченный по качеству назначен приказом по предприятию.
В наш Центр часто обращаются руководители аптек за консультацией с просьбой разъяснить, какие вопросы относятся к ведению уполномоченного по качеству, каковы его должностные обязанности, ответственность.
Уполномоченный по качеству должен руководствоваться основами законодательства о здравоохранении, труде, знать нормативную правовую базу, регламентирующую фармацевтическую деятельность, владеть теоретическими основами системы подтверждения соответствия, уметь практически осуществлять управление и контроль качества лекарственных средств, знать организацию и технологию всех производственных процессов аптеки.
ДОЛЖНОСТНЫЕ ОБЯЗАННОСТИ УПОЛНОМОЧЕННОГО ПО КАЧЕСТВУ
В общих чертах можно сказать, что уполномоченный по качеству в соответствии с ОСТом 91500.05.0007-2003 курирует следующие вопросы:
Должностные обязанности уполномоченного по качеству обширны, охватывают многие стороны фармацевтической деятельности аптеки и в крупных аптечных сетях часть обязанностей могут быть перераспределены между другими специалистами, такими как менеджер по персоналу, руководители структурных подразделений и др.
В должностные обязанности уполномоченного по качеству входит:
Уполномоченный по качеству должен обеспечить упорядоченное хранение правоустанавливающих документов или их копий на объект недвижимости, заключения санитарной и противопожарной службы, документы на оборудование, имеющееся в аптеке. В соответствии с Отраслевым стандартом помещения аптеки должны быть оснащены мебелью и технологическим оборудованием, разрешенным к применению; все приборы и аппараты, используемые в аптеке, должны регулярно проходить проверку и иметь технические паспорта, сохраняющиеся в течение всего времени эксплуатации.
Работа уполномоченного по качеству с поставщиками
Очень важным моментом в деятельности аптечной организации является определение поставщиков и закупка лекарственных средств и другой медицинской продукции. Уполномоченный по качеству может привлекаться к разработке договора поставки в части формирования требований раздела по качеству и комплектности поставляемой продукции. В этом разделе должны быть определены требования к поставляемой продукции, их качеству, комплектности, срокам годности, сопроводительной документации по качеству, порядку приемки товаров и возврату/замене продукции, не отвечающей требованиям качества. В договоре поставки необходимо предусмотреть порядок приемки товара по количеству и качеству, установленный Инструкцией о порядке приемки продукции производственно-технического назначения и товаров народного потребления по количеству, утвержденной Постановлением Госарбитража СССР от 15.06.65 №П-6 и Инструкцией о порядке приемки продукции производственно-технического назначения и товаров народного потребления по качеству, утвержденной Постановлением Госарбитража СССР от 25.04.66 №П-7.
Приемка и приемочный контроль продукции, поступающей в аптеку, производится уполномоченными на то лицами в соответствии с требованиями Отраслевого стандарта ОСТ 91500.05.0007-2003, утвержденного приказом МЗ РФ от 04.03.2003 г. №80, приказом МЗ РФ от 16.07.97 №214 «О контроле качества лекарственных средств, изготовляемых в аптеках», инструкциями о порядке приемки продукции по количеству, качеству.
Нет необходимости подробно раскрывать эти вопросы в рамках данной статьи.
Однако хочется еще раз напомнить, что согласно «Инструкции по контролю качества лекарственных средств, изготовляемых в аптечных организациях (аптеках)», утвержденной Приказом Минздрава РФ от 16.07.97 №214 «О контроле качества лекарственных средств, изготовляемых в аптеках» приемочный контроль заключается в проверке поступающих лекарственных средств на соответствие требованиям по показателям: «Описание»; «Упаковка»; «Маркировка»; в проверке правильности оформления расчетных документов (счетов), а также наличия сертификатов соответствия производителя и других документов, подтверждающих качество лекарственных средств в соответствии с действующими нормативными документами.
В случае сомнения в качестве ЛС образцы направляются в территориальную испытательную лабораторию. Такие ЛС с обозначением: «Забраковано при приемочном контроле» хранятся в аптеке изолированно от других лекарственных средств.
Аптечная организация не имеет в своем арсенале Государственного реестра лекарственных средств, нормативной документации, устанавливающей требования по данным показателям, кроме того, в аптеку ЛС поставляются с приложением только сведений о подтверждении соответствия (без приложения документов), в большинстве аптечных предприятий отсутствуют базы данных по забракованным и фальсифицированным препаратам.
В настоящее время во всем мире очень остро стоит вопрос фальсификации продукции, в т.ч. и ЛС. Кроме того, лекарственное средство проходит через длинную цепочку дистрибьюторов и на каждом этапе возможна порча препаратов, поэтому проведение приемочного контроля в полном объеме является очень важной процедурой.
Так, в 2009 г. Нижегородским областным центром по контролю качества и сертификации лекарственных средств проведен мониторинг качества 247 641 партии лекарственных средств, из них 66 партий имели несоответствия по показателям «Описание», «Упаковка», «Маркировка», что составило 78 053 упаковки, а 2010 г. прошли мониторинг качества 234 898 партий, из них 92 не соответствовали требованиям нормативной документации, объем этих партий составил 215 199 упаковок.
Весь этот объем забракованной продукции возник по вине оптовых поставщиков.
К сожалению, в аптеке не всегда есть возможность проверить поступивший товар по базам забракованных и фальсифицированных препаратов, провести идентификацию деклараций о соответствии, обратить пристальное внимание на те ЛС, которые наиболее часто значатся в числе фальсифицируемых, да и обнаружить признаки фальсификата фармацевту аптеки практически невозможно (для этого нужны сведения по отличительным признакам, специальные приборы и опытные специалисты). При том обилии ЛС, которые ежедневно получает аптека, проведение тщательного приемочного контроля затруднительно.
Хочется отметить, что все эти процедуры, а именно:
осуществляют региональные Центры контроля качества лекарственных средств в рамках мониторинга качества лекарств, ввозимых на территорию субъекта, проводимом на основании договоров, заключенных с поставщиками лекарственной продукции.
Фактически региональные Центры контроля качества ЛС оказывают большую помощь работникам аптек, т.к. препараты, подвергшиеся мониторингу качества при ввозе на территорию субъекта, прошли детальный приемочный контроль специалистами в области контроля качества ЛС.
ПРИЕМОЧНЫЙ КОНТРОЛЬ И ХРАНЕНИЕ
Четкая организация приемки, приемочного контроля и хранения продукции являются основополагающими аспектами в обеспечении качества ЛС аптечным предприятием.
После проведения приемки и приемочного контроля, лекарственные средства должны быть размещены по местам хранения в соответствии с требованиями приказа Минздравсоцразвития от 23.08.10 №706н «Об утверждении правил хранения лекарственных средств», с учетом их физических и физико-химических свойств, воздействия на них различных факторов внешней среды.
Хранение изделий медицинского назначения должно быть организовано в соответствии с приказом Минздрава РФ от 13.11.96 №377 «Об утверждении требований к организации хранения в аптечных организациях различных групп лекарственных средств и изделий медицинского назначения» (в ред. Приказа Минздравсоцразвития от 23.08.10 №706н).
Приказом Минздравсоцразвития от 23.08.10 №706н «Об утверждении правил хранения лекарственных средств» предусмотрена идентификация товара с помощью стеллажной карты. Допускается идентификация товара с применением компьютерных технологий при помощи кодов.
В помещениях хранения ЛС обязательным является наблюдение и фиксация в соответствующих журналах или в электронном виде показателей температуры и относительной влажности воздуха.
Контролю должен подвергаться и температурный режим в холодильниках. Контролирующие приборы должны быть сертифицированы, калиброваны и подвергаться проверке в установленном порядке.
В аптеке должен вестись учет лекарственных препаратов с ограниченным сроком годности.
ВЕДЕНИЕ ДОКУМЕНТАЦИИ ПО КОНТРОЛЮ КАЧЕСТВА
С целью надлежащего функционирования системы управления качеством для специалистов аптечной организации должны быть разработаны четкие инструкции на всех этапах обращения продукции (порядок приемки товара, приемочного контроля, порядок возврата продукции ненадлежащего качества, инструкция по организации хранения товара, контроля температурного режима и сроков годности, инструкции по санитарному режиму аптеки и другие процедуры, исходя из спектра услуг, оказываемых аптекой). Уполномоченный по качеству принимает самое активное участие в разработке этих документов.
Все перечисленные вопросы, а именно: порядок приемки товара, проведение приемочного контроля, организация хранения и соблюдение условий хранения, перемещения, изготовления и отпуска лекарственных средств, ведение необходимой учетной документации, хранение накладных и приложений к ним, контролирует уполномоченный по качеству.
Уполномоченный по качеству контролирует соблюдение санитарного режима на аптечном предприятии в соответствии с действующими нормативными документами и своевременное прохождение ежегодных медицинских осмотров.
Очень важным разделом в работе уполномоченного по качеству является проведение мероприятий, направленных на противодействие поступлению в аптеку недоброкачественной и фальсифицированной продукции, а именно:
За редким исключением работа с информацией по качеству ЛС, а также сведениями о забракованной и фальсифицированной продукции в аптеках не имеет системного характера. Ответственные за этот раздел лица просматривают публикации Территориального управления Росздравнадзора и Центра контроля качества лекарственных средств в специализированных периодических изданиях или на соответствующих сайтах, при этом формирование постоянно обновляемых баз данных по браку и фальсификатам внутри аптечного предприятия не происходит. Данная ситуация дает возможность проникновению в реализацию недоброкачественных и фальсифицированных препаратов. Хотя в ряде крупных аптечных сетей Нижегородской обл. созданы собственные программные продукты, содержащие вышеназванные базы ЛС, которые позволяют остановить фальсификат и брак на этапе поступления товара в аптеку, а также в дальнейшем изымать из обращения некачественную продукцию при получении соответствующей информации от Росздравнадзора. При создании таких программ аптечные предприятия используют базу данных по браку и фальсификату, сформированную нашим Центром начиная с 2000 г. и сегодня обновление осуществляется за счет сведений, обобщенных и систематизированных ГУЗ НОЦККСЛС.
Хочется сказать, что региональные Центры контроля качества ЛС имеют базы данных забракованных и фальсифицированных лекарственных средств, регулярно их обновляют и могут оказать аптечным предприятиям большую помощь в формировании таких данных и постоянное их пополнение.
В аптеке должен быть определен порядок действий при выявлении недоброкачественной и фальсифицированной лекарственной продукции, в котором следует четко определить следующие моменты:
Необходимо определить ответственных лиц, а также сроки предоставления информации и отчетности о проведенных мероприятиях.
Документация на персонал должна включать копии дипломов, сертификатов специалистов, трудовых договоров, приказов о назначении на должность, должностных инструкций.
Уполномоченный по качеству формирует график последипломного обучения персонала, контролирует своевременное повышение квалификации специалистов, подтверждение сертификатов и квалификационных категорий.
Уполномоченный по качеству организует проведение занятий по повышению деловой квалификации (техучебы) для персонала, определяет темы для рассмотрения на занятиях, готовит материалы и привлекает специалистов для проведения техучебы, следит за выходом новых нормативных документов в области здравоохранения, знакомит с ними персонал аптеки.
Документация по организации занятий по повышению деловой квалификации включает следующее:
Уполномоченный по качеству планирует и проводит внутренние проверки на соответствие требованиям нормативных документов, регламентирующих фармдеятельность. Периодичность проверок определяется самой аптечной организацией. При проведении проверок следует обращать внимание на наличие рабочих инструкций на каждом участке производственного процесса и на их соблюдение, а также устранение недостатков, выявленных в ходе предыдущих проверок. По результатам проверки составляется протокол, где указываются рекомендации и сроки устранения недостатков. Результаты проверок доводятся до сведения руководителя предприятия и ответственных лиц.
По результатам внутренних проверок в целях повышения эффективности системы управления качеством могут вноситься изменения и дополнения в должностные инструкции, документированные процедуры.
Таким образом, руководитель аптеки должен очень тщательно подходить к подбору кандидатуры на должность уполномоченного по качеству, поскольку в его обязанности входит контроль за всеми процессами, осуществляемыми аптекой, и на нем лежит ответственность за допущенные нарушения фармдеятельности.
Технологии и дизайн принадлежат НП РГ «Московские аптеки». Использование материалов сайта (распространение, воспроизведение и др.) допускается только с письменного разрешения редакции. Для интернет-изданий - активная ссылка на mosapteki.ru
Вся информация предназначена только для специалистов здравоохранения и сферы обращения лекарственных средств и не может быть использована пациентами при принятии решения о применении описанных методов лечения и продуктов.
Информация на сайте не должна быть использована как призыв к неспециалистам самостоятельно приобретать или использовать описываемые продукты.
© НП РГ «Московские аптеки» 2013 - 2016 v.2.11.16173