










 Рейтинг: 4.5/5.0 (1914 проголосовавших)
Рейтинг: 4.5/5.0 (1914 проголосовавших)Категория: Инструкции

Главная | О нас | Обратная связь
Стандартизация - это установление в государственном порядке или внутри отрасли строго определенных норм качества сырья, продукции, методов испытаний, обязательных для производителей и потребителей. Контроль качества лекарственного растительного сырья возможен только при наличии определенных стандартов, сравнением с которыми определяется уровень разработки, испытаний и производства из него лекарственных средств. Установленные нормы и требования на лекарственное растительное сырье изложены в разнообразных стандартах, часто обобщенно называемых нормативными документами.
В настоящее время основными документами, определяющими подлинность, чистоту и доброкачественность лекарственного растительного сырья, являются: Государственная фармакопея (ГФ), фармакопейные статьи (ФС), фармакопейные статьи предприятия
(ФСП), государственный стандарт (ГОСТ), отраслевые стандарты (ОСТ), технические условия (ТУ), международные требования (комплекс требований GMP 1 ).
Требования, указанные в документах и предъявляемые к лекарственному растительному сырью, обязательны для всех предприятий и учреждений Российской Федерации, изготовляющих, хранящих, контролирующих и применяющих лекарственные средства.
Государственная фармакопея и фармакопейные статьи всех категорий имеют силу государственных стандартов и утверждаются профильным министерством. Государственная фармакопея - это сборник обязательных общегосударственных стандартов и положений, нормирующих качество лекарственных средств и лекарственного сырья. Она имеет законодательный характер. В Государственную фармакопею включаются фармакопейные статьи на лекарственное растительное сырье, имеющее наибольшую терапевтическую ценность, высокие качественные показатели и широко вошедшие в медицинскую практику.
Стандарт GMP (Good Manufactoring Practice, надлежфщая производственная практика)– система норм, правил и указаний в отношении производства лекарственных средств, медицинских устройств, изделий диагностического назначения, продуктов питания, пищевых добавок и активных ингредиентов. В отличие от процедуры контроля качества путем исследования выборочных образцов таких продуктов,которая обеспечивает пригодностьк использованию лишь самих исследуемых образцов (и, возможно, партий, изготовленных в ближайшее к данной партии время) стандарт GMP отражает целостный подход и регулирует и оценивает собственно параметры производства и лабораторной практики.
Лекарственные растения, включенные в Государственную фармакопею, называются официнальными (от латинского officina - аптека). Лекарственные растения, не включенные в фармакопею, рассматриваются как неофицинальные и включены в другие нормативные документы.
Фармакопейные статьи утверждаются на лекарственные средства и лекарственное растительное сырье серийного производства, разрешенные для медицинского применения и включенные в Государственный реестр. В Государственную фармакопею входят только те статьи, которые хорошо проверены на практике. Но статьи, исключенные из нового издания Государственной фармакопеи, при необходимости (например, при импорте препарата или сырья) имеют юридическую силу. Государственная фармакопея и фармакопейные статьи должны пересматриваться не реже одного раза в 5 лет.
Фармакопейные статьи предприятия создаются производителями лекарственных препаратов и являются их интеллектуальной собственностью. Основой для ФСП служат соответствующие фармакопейные статьи, однако они могут различаться некоторыми требованиями к качеству сырья. Однако требования, предъявляемые в ФСП к показателям и методам контроля качества лекарственного растительного сырья, должны быть не ниже требований, изложенных в ГФ.
ГОСТ - это государственный стандарт, документ, определяющий качественные нормы сырья, изделий и регламентирующий условия, необходимые для его сохранения; упаковки, маркировки. ГОСТ, как и ФС, имеет шифр - товарную нумерацию. ГОСТ устанавливается на объекты, имеющие не только лекарственное, но и техническое применение в других отраслях промышленности: лакокрасочной, парфюмерной, пищевой и т. д.
ОСТ - отраслевой стандарт, так же как и ГОСТ, определяет качественные нормы сырья, изделий и регламентирует условия, необходимые для его сохранения. Отраслевые стандарты бывают методические, включающие общие методы приемки, испытаний, правила упаковки, маркировки, транспортирования и хранения лекарственного растительного сырья, и стандарты на промежуточную продукцию, выпускаемую соответствующей отраслью, но не поступающую потребителю.
Технические условия составляются на лекарственное сырье, заготовляемое в большом количестве, но не имеющее серийного производства.
Нормативно-техническая документация должна контролировать качество лекарственных средств с учетом достижений науки и техники, передового опыта и своевременно пересматриваться.
Анализ на соответствие требованиям нормативного документа проводят на аптечных складах (базах) и на предприятиях, перерабатывающих лекарственное сырье или изготавливающих из него лекарственные средства.
Т12 Табакова Т.Д. Смирнова В.В. Общая рецептура. Учебное пособие. – 4-е изд. перераб. и доп. – Тверь: Издательство «Фамилия», 2007. – 96 с.
В данном учебном пособии приводятся общие вопросы рецептуры, описано более 50 лекарственных форм и их разновидностей, даны 128 рецептурных прописей, 9 таблиц.
Для студентов-медиков и врачей.
Решением Центрального координационно-методического Совета Тверской государственной медицинской академии от 21.02.2002 г. пособию присвоен гриф ТГМА.
Табакова Татьяна Дмитриевна – кандидат медицинских наук, доцент кафедры фундаментальной и клинической фармакологии ТГМА.
Смирнова Валентина Васильевна – кандидат медицинских наук, старший преподаватель кафедры фундаментальной и клинической фармакологии ТГМА.
Базанов Геннадий Александрович – доктор медицинских наук, профессор, академик РАЕН, заведующий кафедрой фундаментальной и клинической фармакологии ТГМА.
Художественный редактор и компьютерный дизайнер:
Бармин Дмитрий Альфредович – кандидат медицинских наук, доцент кафедры фундаментальной и клинической фармакологии ТГМА.
Демидова Марина Александровна – доктор медицинских наук, профессор, заведующая кафедрой управления и экономики фармации ТГМА.
Аникин Виктор Васильевич – доктор медицинских наук, профессор, заведующий кафедрой пропедевтики внутренних болезней ТГМА.
Гнусаев Сергей Федорович – доктор медицинских наук, профессор, заведующий кафедрой педиатрии № 2 ТГМА.
ISBN 5-88662-028-1 © Кафедра фундаментальной и клинической фармакологии ТГМА, 2007
ВВЕДЕНИЕ В ОБЩУЮ РЕЦЕПТУРУ
Современное лекарствоведение представляет собой комплекс самостоятельных научных отраслей и дисциплин, в котором можно выделить 2 основные науки: фармакологию и фармацию.
Фармакология – наука, изучающая взаимодействие лекарственных веществ с живыми организмами, а именно: влияние лекарств на биохимические, физиологические, морфологические процессы в организме и, с другой стороны, регуляцию организмом действия лекарств. Кроме того, в задачу фармакологии входит поиск новых, более совершенных лекарственных средств.
Фармация – научно-практическая отрасль, занимающаяся вопросами изыскания и приготовления лекарственных средств. Основными разделами фармации являются фармакогнозия – наука о лекарственном сырье растительного и животного происхождения, фармацевтическая химия . изучающая химические лекарственные средства, фармацевтическая технология . занимающаяся разработкой и совершенствованием лекарственных форм, управление и экономика фармации . рецептура. Рецептура изучает правила выписывания лекарств в рецептах (общая или врачебная рецептура) и правила их приготовления (фармацевтическая рецептура). Настоящее пособие посвящено вопросам общей рецептуры.
Все названные науки с разных точек зрения изучают лекарства или лекарственные вещества. Лекарственное вещество – это вещество, используемое для лечения заболеваний, их профилактики или диагностики. Источниками получения лекарств являются минеральное сырье, растения, органы и ткани животных, их активные субстанции, а также продукты бактериального и грибкового происхождения. В настоящее время многие лекарственные вещества создают синтетическим путем. С 80-х годов ХХ века лекарства получают и с помощью биотехнологии (генной инженерии).
Для удобства применения больными лекарственные вещества заключают в соответствующие лекарственные формы: твердые, мягкие, жидкие. Лекарственные вещества в определенной лекарственной форме называют лекарственными препаратами.
Лекарственное обеспечение населения осуществляется через оптовую и розничную торговлю. Оптовой торговлей занимаются производители лекарственных средств или предприятия оптовой торговли при наличии лицензии на данный вид деятельности. Розничная торговля лекарственными средствами проводится аптечными учреждениями разных форм собственности (государственная, муниципальная, частная). К аптечным учреждениям относятся аптеки, аптечные пункты, магазины и киоски.
Аптека – это учреждение, осуществляющее розничную торговлю готовыми лекарственными средствами, а также изготовление и отпуск лекарств по рецептам врачей. Первая аптека была открыта в 754 г. в Багдаде (Ирак). В России аптечное дело развивается с 1581 г.
Аптека может иметь 3 отдела: 1) рецептурно-производственный, 2) отдел готовых форм, 3) отдел ручной продажи.
Эти отделы работают с населением в приемной комнате. Вотделе ручной продажи отпускаются лекарства без рецептов, а также предметы санитарии и гигиены. Отдел готовых форм выдает по рецептам лекарственные средства, выпускаемые фармацевтической промышленностью. Рецептурно-производственный отдел занимается изготовлением и отпуском лекарственных форм по рецептам. В нем выделяют рецептурный отдел . где принимаются рецепты от больных, проверяется их правильность. Лекарственные формы готовятся в ассистентской . Для контроля за качеством изготовляемых лекарств существует контрольно-аналитическая лаборатория . В некоторых аптеках имеется кокторий – специальное помещение для получения дистиллированной воды, приготовления настоев и отваров. Если аптека готовит стерильные лекарственные формы, выделяют асептический блок . Запасы медикаментов для работы аптеки хранятся в материальной . В аптеке имеются моечная – помещение для мытья аптечной посуды, подвал и другие подсобные помещения. В настоящее время многие аптеки специализируются только на отпуске готовых лекарственных форм и не имеют рецептурно-производственного отдела.
В аптеке работают фармацевты – лица со специальным фармацевтическим образованием. Фармацевты с высшим образованием имеют звание провизора . Сотрудники, ответственные за прием рецептов и отпуск по ним лекарств, называются рецептарами . Должность фармацевта, отпускающего лекарства без рецептов, в порядке ручной продажи, называется ручнист . Приготовлением лекарственных форм в аптеке занимаются аптечные ассистенты;контролеры осуществляют контроль за качеством приготовленных лекарств. Запасами медикаментов и сырья для приготовления лекарственных препаратов ведает дефектар . Вспомогательный аптечный персонал составляют лица, не имеющие специального образования: фасовщики, кассиры и др.
Аптечным работникам и врачам известно, что лекарственные вещества неоднородны по активности. Это имеет значение при выписывании, работе с лекарствами и их хранении.
Существуют лекарственные средства, отпускаемые без рецепта врача
– средства от головной боли, отхаркивающие, жаропонижающие вещества, многие средства местного действия, растения.
Лекарственные средства рецептурного отпуска в настоящее время подразделяют на 3 группы. списки А и Б, списки сильнодействующих и ядовитых веществ Постоянного комитета по контролю наркотиков (ПККН), списки Перечня наркотических, психотропных веществ и их прекурзоров, подлежащих контролю в Российской Федерации, введенные в соответствии с Федеральным Законом №3 «О наркотических и психотропных веществах» от 8.01.98 г.
Список А включает многие ядовитые вещества медиаторного действия (например, пилокарпин, атропин, курареподобные препараты), противоопухолевые средства, сердечные гликозиды и др. Список Б – наиболее обширный и содержит основные лекарственные вещества из группы нейротропных средств, веществ, влияющих на исполнительные органы, обменные процессы, средств для лечения инфекций.
ПККН ввел 2 вида списков лекарств: список №1 сильнодействующих веществ (эфир для наркоза, тиопентал-натрий, фенобарбитал, диазепам, трамадол, нандролон и др.) и список №2 ядовитых веществ (мышьяковистый ангидрид, ртути дихлорид, стрихнина нитрат, алкалоиды красавки и др.), причем списки ПККН включают на только лекарственные вещества.
Перечень наркотических средств, психотропных веществ и их прекурзоров. подлежащих контролю в РФ, состоит из 4-х списков.
Список I включает наркотические и психотропные вещества, оборот которых в РФ запрещен. Например: героин, каннабис (марихуана), фенадон и др.
Список II включает наркотические и психотропные вещества, оборот которых в РФ ограничен и в отношении которых устанавливаются меры контроля в соответствии с законодательством РФ и международными договорами. Например: морфин, кодеин, кокаин, кетамин и др.
Список III включает психотропные вещества, оборот которых в РФ ограничен и в отношении которых допускается исключение некоторых мер контроля в соответствии с законодательством РФ и международными договорами. Например: галотан (фторотан), натрия оксибутират, мазиндол и др.
Список IV – прекурзоры (вещества, используемые при производстве наркотических и психотропных средств), оборот которых в РФ ограничен и в отношении которых устанавливаются меры контроля в соответствии с законодательством РФ и международными договорами. Например: ангидрид уксусной кислоты, лизергиновая кислота, перманганат калия, эфедрин и др.
Списки ПККН, Перечня лекарств Федерального закона №3, некоторые вещества списков А и Б, спирт этиловый подлежат в аптечных учреждениях предметно-количественному учету (ПКУ).
Особые предосторожности соблюдаются при хранении наркотических и психотропных веществ. Наркотические средства должны храниться в сейфе, находящемся в специально оборудованном помещении, снабженном сигнализацией; сейф должен быть опечатан. В аптеке и лечебных учреждениях ведется строгий учет получения и расходования наркотических и психотропных веществ с записями в особом журнале; выделяется сотрудник, ответственный за их хранение и расходование. Скоропортящиеся, огнеопасные вещества и растительное сырье хранятся в холодильниках и подвалах.
Фармакопея – это сборник государственных стандартов качества лекарственных средств, имеющий законодательный характер. Фармакопея включает все необходимые сведения о лекарственных веществах, допущенных к применению в данной стране. Каждому применяющемуся в медицине средству посвящена отдельная фармакопейная статья (ФС). В фармакопейных статьях приводятся описание физико-химических свойств лекарств, качественные и количественные реакции на испытание их подлинности и чистоты, указываются дозы лекарств и условия их хранения. В фармакопее содержатся также методы определения активности лекарств, в том числе их биологической стандартизации, дается описание технологии изготовления всех лекарственных форм.
Непосредственное рабочее значение фармакопея имеет для фармацевтов, поскольку это – руководство по приготовлению лекарственных препаратов, контролю за их качеством. Для врача фармакопея имеет справочное значение: в фармакопее приводится много справочного материала (таблицы доз ядовитых и сильнодействующих веществ для взрослых и детей, таблицы капель, методы математической статистики и т.д.).
Требования фармакопеи являются обязательными для всех предприятий и учреждений страны, изготавливающих и применяющих лекарственные средства. По мере обновления лекарственного арсенала выпускаются новые издания фармакопеи. В РФ в 1987 г. вступило в силу ХI издание фармакопеи (ГФ ХI) .
Для медицинских и фармацевтических товаров утверждаются нормативно-технические документы.
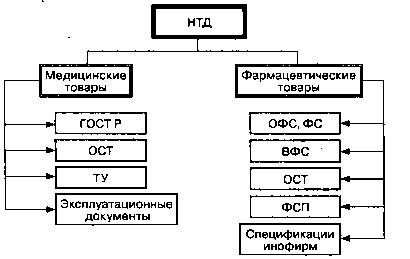
Нормативно-техническая документация на медицинские и фармацевтические товары
В 1973 г. был утвержден ГОСТ 19126-73 на медицинские инструменты. В нем установлены общие технические требования, которым должны соответствовать инструменты, методы контроля показателей и методы испытания инструментов, правила маркировки, упаковки, транспортировки, хранения .
В 1975 г. был утвержден ГОСТ 20790-75 «Приборы, аппараты и оборудование медицинские. Общие и технические условия». Имеются ГОСТы на перевязку, шприцы, иглы, режущие и зажимные инструменты и т.д.
Отраслевые стандарты утверждаются МЗ РФ и обязательны для предприятий и организаций медицинской промышленности.
Контроль качества готовых медицинских товаров осуществляется в соответствии с ТУ.
ТУ на медицинские изделия состоят из следующих разделов:
а) назначение изделия;
в) основные размеры;
г) технические требования;
д) комплектность изделия;
е) правила приемки и методы испытаний;
Стандарт качества лекарственных средств (ЛС) — это нормативный документ, содержащий перечень нормируемых показателей и методов контроля качества ЛС, утверждаемый МЗ РФ.
Для ЛС и лекарственного растительного сырья применяются следующие виды НТД: общие фармакопейные статьи (ОФС), фармакопейные статьи (ФС), временные фармакопейные статьи (ВФС), ОСТ, фармакопейные статьи предприятий (ФСП).
ОФС — государственный стандарт качества ЛС; включает в себя перечень нормируемых показателей или методов испытания для конкретной лекарственной формы, описание физических, физико-химических, химических, биохимических, биологических, микробиологических методов анализа ЛС, требования к используемым реактивам, титрованным растворам, индикаторам.
ФС — государственный стандарт качества ЛС под международным непатентованным наименованием (МНН), содержит обязательный перечень показателей и методов контроля качества с учетом его лекарственной формы.
ФС утверждаются на ЛС, имеющие наибольшую терапевтическую ценность, широко вошедшие в медицинскую практику и имеющие высокие качественные показатели. ФС включаются в государственную фармакопею (серийное производство ).
Термин «Фармакопея» происходит от греческих словpharmakon — лекарство и poieo — делаю и переводится на русский язык как руководство по приготовлению лекарств.
Государственная фармакопея (ГФ) — это сборник государственных стандартов качества ЛС, имеющий законодательный характер. В настоящее время действует ГФ XI издания (1987).
ВФС утверждаются на ЛС и лекарственное растительное сырье и на первые промышленные серии новых ЛС, рекомендованных к медицинскому применению фармакопейным комитетом и намеченных к серийному производству. Утверждаются на ограниченный срок (не более 3 лет).
ОСТ устанавливаются на дополнительные технические требования и групповые характеристики, необходимые для изготовления и поставки ЛС (термины, обозначения, правила приемки, маркировка,
упаковка. хранение, транспортирование и др.); утверждаются МЗ РФ и медицинской промышленности.
ФСП — стандарт качества на ЛС под торговым названием, содер-кащий перечень показателей и методов контроля качества ЛС, произведенного конкретным предприятием, учитывающий конкретную технологию данного предприятия и прошедший экспертизу и регистрацию в установленном порядке.
Многие страны имеютсвои национальные фармакопеи, с 1951 г. ПОЗ издает международную фармакопею. В настоящее время вышло три ее издания (1967, 1981, 1988). Международная фармакопея состоит из 5 томов: том 1 содержит общие методы анализа; 2 и 3 тома содержат спецификации для контроля качества фармакопейных препаратов (том 2 — 126 субстанций, том 3 - 157 субстанций); 4 и 5 тома содержат спецификации для контроля качества готовых лекарственных форм, вспомогательных средств и упаковочных материалов.
Для импортных ЛС к НТД относятся:
2) зарубежные фармакопеи;
3) спецификации (статьи, нормы, сертификаты качества), разработанные иностранными фирмами.
Помимо НТД, есть еще эксплуатационные документы. которые входят в комплект изделия при выпуске их с предприятия-изготовителя. К простым изделиям, хорошо известным потребителям, прилагается этикетка (наименование изделий, обозначение изделия и его индекс, технические данные, номер стандарта или ТУ, которым соответствует изделие, сведения о приемке ОТК, сведения о количестве изделий в одной упаковке, дата выпуска).
К сложным изделиям прилагаются паспорта или формуляры.
В паспорте указывают основные параметры и характеристики изделия, далее приводятся данные, аналогичные сведениям в этикетке, гарантийные обязательства предприятий, сведения о консервации и упаковке.
Если к паспорту прилагаются журнал или листки, в которых указывается работа изделия и сведения о техническом обслуживании, то эти документы носят название формуляр. В необходимых случаях к эксплуатационным документам прилагается техническое описание (ТО), инструкция по эксплуатации (ИЭ); иногда их объединяют.
ПопулярноеФармакопе?я (с др.-греч. ???????? — лекарство. яд и др.-греч. ???? — делаю, изготовляю) — сборник официальных документов (свод стандартов и положений), устанавливающих нормы качества лекарственного сырья — медицинских субстанций, вспомогательных веществ, диагностических и лекарственных средств и изготовленных из них препаратов.
Положения фармакопеи основаны на достижениях фармацевтической химии и ее фармацевтического анализа, его критериев, способов и методов [1]. Этот документ включает указания по изготовлению, проверке качества лекарств. Определяет высшие дозы препаратов и устанавливает требования к лекарственному сырью. Выполнение изложенных норм и требований Фармакопеи в сочетании с исполнением требований стандарта GMP обеспечивает надлежащее качество лекарственных субстанций и препаратов.
Государственная фармакопея — фармакопея, находящаяся под государственным надзором. Государственная фармакопея является документом общегосударственной законодательной силы, его требования обязательны для всех организаций данного государства, занимающихся изготовлением, хранением и применением лекарственных средств, в том числе растительного происхождения.
Содержание ИсторияИстория сборников материалов по фармации восходит к древним рукописям, среди которых известны Папирус Эдвина Смита. фармакопея Плиния Старшего. Сад Здравия Петера Шёффеля и другие.
Многие страны имеют собственные фармакопеи. Всемирная организация здравоохранения издаёт Международную Фармакопею, не имеющую, однако, законодательного характера, в отличие от национальных фармакопей. В странах, не имеющих собственных фармакопей, используют международную, европейскую или другую. Многие химико-фармацевтические предприятия выпускают субстанции по требованию заказчика — в соответствии с заданным стандартом, с той или иной фармакопеей.
РоссияСоставление, дополнение и переиздание Фармакопеи ранее осуществлялось фармакопейным комитетом. В настоящее время Фармакопею готовит редакционный совет, в который входят представители Минздравсоцразвития. Росздравнадзора, Росздрава. ФФОМС и ведущие российские учёные.
Соединенные Штаты Америки Великобритания ГерманияВ Германии действуют 3 Фармакопеи:
Государственная фармакопея Украины I (ГФУ) выпущена в 2001 году, четыре дополнительных тома — в 2004, 2008, 2009 и 2011 годах, соответственно. Украинская фармакопея фактически по частям воспроизводит Европейскую Фармакопею .
БелоруссияГосударственная фармакопея Республики Беларусь (ГФ РБ), гармонизирована с Европейской Фармакопеей и включает три тома:
Головная организация-разработчик - Республиканское унитарное предприятие «Центр экспертиз и испытаний в здравоохранении».
Международная и региональная фармакопеиФАРМАКОПЕЯ — греч. от pharmakon, лекарство, и poieo, делаю. Приготовление лекарств. Объяснение 25000 иностранных слов, вошедших в употребление в русский язык, с означением их корней. Михельсон А.Д. 1865. ФАРМАКОПЕЯ обязательное для аптекарей руководство к… … Словарь иностранных слов русского языка
ФАРМАКОПЕЯ — (от греческого pharmakon лекарство и poieo делаю), сборник стандартов и положений, регламентирующих требования к качеству лекарственных средств. 1 я фармакопея издана в 1498 во Флоренции. В России 1 я фармакопея (на латинском языке) вышла в 1778; … Современная энциклопедия
ФАРМАКОПЕЯ — (от греч. pharmakon лекарство и poieo делаю) сборник стандартов и положений, регламентирующих требования к качеству лекарственных средств. 1 я Фармакопея издана в 1498 во Флоренции. В России 1 я Фармакопея (на латинском языке) вышла в 1778; в… … Большой Энциклопедический словарь
Фармакопея — (от греческого pharmakon лекарство и poieo делаю), сборник стандартов и положений, регламентирующих требования к качеству лекарственных средств. 1 я фармакопея издана в 1498 во Флоренции. В России 1 я фармакопея (на латинском языке) вышла в 1778; … Иллюстрированный энциклопедический словарь
ФАРМАКОПЕЯ — (от греч. pharmakon лекарство и poieo делаю), сборник стандартов лекарственных препаратов и предписаний об изготовлении нек рых лекарственных форм. Издание первой официальной книги подобного рода относится к 9 в. (арабский Крабаддин). В России… … Большая медицинская энциклопедия
ФАРМАКОПЕЯ — ФАРМАКОПЕЯ, фармакопеи, мн. нет, жен. (от гроч. pharmakon лекарство и poieo делать) (спец.). Официальное руководство для фармацевтов, содержащее описание способов приготовления, хранения, проверки лекарств, перечень лекарственных веществ, которые … Толковый словарь Ушакова
ФАРМАКОПЕЯ — ФАРМАКОПЕЯ, и, жен. (спец.). Свод обязательных правил, к рыми руководствуются при изготовлении, проверке, хранении и назначении больным лекарственных препаратов. | прил. фармакопейный, ая, ое. Толковый словарь Ожегова. С.И. Ожегов, Н.Ю. Шведова.… … Толковый словарь Ожегова
фармакопея — сущ. кол во синонимов: 3 • диспенсатория (2) • сборник (61) • фармакопия (1) … Словарь синонимов
Фармакопея — книга, в которой описаны сырые лекарственные вещества,известные смеси и готовые препараты, которые должны находиться в запасахаптеки, или изготовляться в последней. Обыкновенно Ф. издаетсяправительственным учреждением и имеет значение… … Энциклопедия Брокгауза и Ефрона
фармакопея — Сборник обязательных национальных или региональных стандартов и положений, нормирующих качество лекарственных средств, с указанием способов изготовления, правил отпуска по рецептам врачей, высших доз, правил хранения и т.п.; может также содержать … Справочник технического переводчика
КнигиЦель. Уметь работать с основными нормативными документами и применять их в профессиональной деятельности при обеспечении соответствующих условий изготовления лекарственных препаратов, реализации технологического процесса и контроля качества лекарственных форм.
Работа в лаборатории. Изучить нормативные документы в процессе учебной деятельности, выполняя блок заданий в тестовой форме, решая предложенные преподавателем ситуационные задачи, связанные с конкретной профессиональной деятельностью.
Изучить структуру ГФ и других нормативных документов.
Научиться использовать для решения технологических задач НД, регламентирующие:
• состав лекарственных препаратов, и анализировать правильность выписывания рецептов, предложенных преподавателем;
• условия изготовления лекарственных препаратов;
• контроль качества лекарственных препаратов.
Оснащение. Нормативные документы: Федеральный закон «О лекарственных средствах» от 22.06.1998 № 86-ФЗ, ГФ, приказы, инструкции, методические указания, утвержденные Минздравом (Минздравсоцразвития) России, ФС, ФСП, отраслевые стандарты (ОСТы) и др.
Практические умения. После самоподготовки и выполнения заданий в аудитории студенты должны уметь: использовать ГФ, приказы, инструкции и методические указания, утвержденные Минздравом (Минздравсоцразвития) России, при выполнении заданий в тестовой форме обучающего характера, решении ситуационных задач, реализовывать их положения в профессиональной деятельности.
Регламентация права на фармацевтическую деятельность. В соответствии со ст. 17 Федерального закона «О лекарственных средствах» изготовление лекарственных средств осуществляют в аптечном учреждении, имеющем лицензию на фармацевтическую деятельность, по правилам изготовления лекарственных средств, утвержденным федеральным органом контроля качества лекарственных средств.
Физические лица, ответственные за изготовление и качество лекарственных средств (фармацевты и провизоры) и имеющие сертификат, указываются в лицензии на фармацевтическую деятельность и несут дисциплинарную, административную и уголовную ответственность за нарушение Федерального закона «О лекарственных средствах» (ст. 18). Это направление более подробно изучается в курсе управления и экономики фармации.
Регламентация состава лекарственного препарата. Состав препарата, изготавливаемого в аптечном учреждении, регламентируют прописью, которую выписывает врач в рецепте или требовании (в больничных и межбольничных аптеках). Прописи могут быть: а) стандартные (представленные в НД); б) нестандартные (врачебные или магистральные) – в этом случае рецепт является единственным НД.
Правила выписывания рецептов и их структура изложены в приказах Минздравом (Минздравсоцразвития) России «О правилах выписывания рецептов на лекарственные средства и их отпуске» от 23.08.1999 № 328 (в ред. от 09.01.2001 № 3) (прил. 1, 2), «Улучшение учета, хранения, выписывания и использования наркотических лекарственных средств» от 12.11.1997 № 330.
Регламентация технологического процесса.Регламентация условий, обеспечивающих качество лекарственного препарата. Изготовление препаратов, как промышленное, так и аптечное, должно соответствовать GMP (Good manufacturing practics) – Правилам надлежащего производства. Кроме того, аптеки руководствуются положениями Инструкции по санитарному режиму аптечных организаций (аптек), утвержденной приказом Минздрава России от 01.10.1997 № 309. Условия, сроки хранения, режим стерилизации разных препаратов регламентированы Приказом Минздрава России «О контроле качества лекарственных средств, изготовляемых в аптеках» от 16.07.1997 № 214, Методическими указаниями по изготовлению стерильных растворов в аптеке (М. Минздрав России, 1994), ФС и другими НД.
Регламентация условий, обеспечивающих технику безопасности и охрану труда персонала. Персонал аптечных учреждений регулярно проходит медицинское обследование и проверку на бациллоносительство.
Соблюдение ТБ, правил ОТ, условий хранения лекарственных средств (особенно ядовитых, наркотических, огнеопасных, взрывоопасных, летучих, пахучих и других) в специальных шкафах или помещениях позволит обеспечить надлежащие условия работы персонала и предотвратить развитие аллергических и других профессиональных заболеваний.
Правила ТБ изложены в соответствующих должностных инструкциях, а также в ряде нормативных актов – приказах Минздрава (Минздравсоцразвития) России, методических указаниях.
Регламентация технологии изготовления лекарственных препаратов. Собственно технологический процесс регламентирован:
• общими статьями ГФ на лекарственные формы;
• приказами Минздрава России («Об утверждении инструкции по изготовлению в аптеках жидких лекарственных форм», «О контроле качества лекарственных средств, изготовляемых в аптеках»);
• методическими указаниями («Методические указания по изготовлению стерильных растворов в аптеке»);
• инструкциями («Инструкция по изготовлению суппозиториев методом выливания в формы») и др.
Регламентация контроля качества лекарственных препаратов. Качество изготовленного препарата может быть обеспечено только при безусловном выполнении требований НД по трем указанным выше направлениям. Кроме того, ряд НД содержит непосредственно нормируемые показатели качества лекарственных средств, вспомогательных веществ, дисперсных сред, изготовленного препарата, при отпуске препарата из аптеки.
Контроль качества изготовленных препаратов регламентируют приказы Минздрава России «О контроле качества лекарственных средств, изготовляемых в аптеках», «О нормах отклонений, допустимых при изготовлении лекарственных средств и фасовке промышленной продукции в аптеках» от 16.10.1997 № 305, Методические указания «Единые правила оформления лекарств, изготовляемых в аптечных учреждениях (предприятиях) различных форм собственности» (М. Минздрав России, 1997).
1. При изготовлении лекарственных препаратов в условиях аптеки не руководствуются, как правило, в качестве основных НД:
а) приказами Минздрава (Минздравсоцразвития) России;
б) методическими указаниями Минздрава (Минздравсоцразвития) России;
в) Государственным регистром;
г) инструкциями Минздрава (Минздравсоцразвития) России;
д) Государственным реестром.
2. Государственная фармакопея:
а) имеет законодательный характер;
б) имеет рекомендательный характер;
в) это сборник инструкций по контролю качества;
г) это сборник обязательных стандартов и положений;
д) является НД только для аптек.
3. Государственной регламентации подлежат:
а) условия изготовления лекарственных препаратов;
б) научный поиск в области создания лекарственных препаратов;
в) контроль качества лекарственных препаратов;
г) изобретательская работа;
д) состав препаратов.
4. Аптечное изготовление отличается от промышленного производства:
а) объемом изготавливаемой продукции;
б) требованиями к качеству вспомогательных веществ;
в) сроками годности готовой продукции;
г) требованиями к качеству лекарственных форм.
5. Норма единовременного отпуска «0,2» установлена:
б) экстракта белладонны;
г) атропина сульфата;
д) эфедрина гидрохлорида.
6. Эфедрина гидрохлорид может быть отпущен по одному рецепту в массе не более, г:
д) той, которая выписана в рецепте.
7. Регламентируют норму единовременного отпуска:
б) экстракта термопсиса;
г) этакридина лактата;
д) эфедрина гидрохлорида.
8. Врач превысил в прописи рецепта разовую или суточную дозу веществ списков А или Б и не оформил это превышение соответствующим образом. В этом случае:
а) препарат не изготавливают;
б) уменьшают массу вещества в соответствии с терапевтической дозой;
в) вещество отпускают в дозе, которая указана в ГФ как высшая;
г) отпускают в половине той дозы, которая указана в ГФ как высшая;
д) отпускают в половине дозы, выписанной в прописи рецепта.
9. К списку наркотических лекарственных веществ относят:
б) экстракт красавки;
г) кодеина фосфат;
д) спирт этиловый.
10. К списку А относят:
б) этилморфина гидрохлорид;
в) натрия барбитал;
г) пилокарпина гидрохлорид;
11. Рецепт на право получения препарата, содержащего наркотическое вещество, выписывается на бланке:
б) специальном розового цвета с водяными знаками с определенной серией и номером;
г) нового образца льготного отпуска.
12. Рецепт, содержащий этиловый спирт, выписывают на бланке:
а) розового цвета с водяными знаками;
г) нового образца льготного отпуска.
13. Недопустимо выписывать амбулаторным больным:
а) анаболические гормоны;
б) эфир для наркоза;
в) морфина гидрохлорид;
14. Не разрешается устанавливать срок действия до одного года на рецепты хроническим больным, содержащие:
а) лекарственные препараты, обладающие анаболической активностью;
б) спиртосодержащие лекарственные препараты индивидуального изготовления;
в) препараты, отпускаемые по льготным и бесплатным рецептам;
г) лекарственные средства, подлежащие предметно количественному учету;
д) все указанные выше лекарственные средства и препараты.
15. Кокаин (в пастах), серебра нитрат (в растворе), мышьяковистый ангидрид (в пастах с содержанием его до 50 % ) стоматолог:
а) не имеет права выписывать;
б) имеет право выписывать в рецепте амбулаторному больному;
в) выписывает, но без последующей выдачи препарата из аптеки пациентам на руки;
г) имеет право выписывать в требовании лечебного учреждения.
16. Сокращение термина «Detur signetur»:
17. В соответствии с НД декоративное оформление и озеленение в аптеке:
б) допускается в непроизводственных помещениях;
18. Санитарный день в аптеках проводят один раз:
19. Генеральную уборку производственных помещений аптеки проводят не реже одного раза:
20. Для мытья рук раковины, предназначенные для мытья посуды, использовать:
в) разрешено технологу.
21. Для обработки рук персонала, занятого изготовлением лекарственных препаратов, после мытья с мылом рекомендуется использовать этанол:
г) в концентрации, полученной от поставщика;
д) в смеси 1:1с глицерином.
22. Право пользоваться раковинами производственных помещений аптеки имеют:
а) мойщики посуды;
б) специалисты, занятые фасовкой;
в) директор аптеки и его заместители;
г) специалисты, занятые изготовлением лекарственных препаратов.
23. Посуду, бывшую в употреблении в инфекционных отделениях больницы, в больничной аптеке:
а) не используют;
в) моют и дезинфицируют;
в) моют, дезинфицируют и используют.
24. В аптеках лечебно-профилактических учреждений дезинфицируют посуду:
а) обязательно всю;
б) поступающую из инфекционного отделения;
в) поступающую из хирургического отделения;
г) поступающую из всех отделений;
д) поступающую из приемного отделения.
25. В ГФ включены методы стерилизации:
а) химический (газовый);
в) термический (воздушный);
г) текучим паром;
д) термический (паровой);
е) на песчаной бане.
26. Трубопроводы из полимерных материалов для подачи воды очищенной на рабочее место технолога обеззараживают:
а) 1 % раствором хлорамина 1 ч;
б) 6 % раствором водорода пероксида 6 ч;
в) острым паром из парового стерилизатора 30 мин.
27. Для дезинфекции ковриков из пористой резины и поролона могут быть использованы растворы:
а) 1 % гипохлорита натрия (60 мин);
б) 3 % водорода пероксида с 0,5 % моющего средства (30 мин);
в) 0,75 % хлорамина Б с 0,5 % моющего средства (30 мин).
28. Раствор кислоты уксусной для дезинфекции обуви персонала:
б) не используют.
29. В производственных помещениях асептического блока должна быть предусмотрена вентиляция:
г) с преобладанием притока воздуха над вытяжкой;
д) с преобладанием вытяжки над притоком.
30. Бактерицидные облучатели экранированного типа могут работать:
а) в присутствии персонала;
б) 12 ч в сутки без выключения;
в) некоторое время с истекшим сроком годности;
г) на высоте не менее 2 м от пола;
д) с установленной мощностью 2,5 Вт на 1 м 3 помещения.
31. Умение сотрудников руководствоваться правилами ТБ и ОТ проверяют:
а) 1 раз в месяц;
б) не реже 1 раза в год;
в) директор аптеки;
г) члены квалификационной комиссии (не менее трех);
д) представители вышестоящей организации.
32. В ГФ действующего издания включены общие статьи на лекарственные формы:
а) эмульсии для внутреннего применения;
33. В ГФ алкоголеметрические таблицы:
в) включать нецелесообразно;
г) запланировано включить.
34. При хранении лекарственных средств, созвучных по названию, с сильно различающимися высшими дозами их не рекомендуется располагать:
а) в соответствии с фармакологическими группами;
б) в алфавитном порядке;
г) в соответствии с физико-химическими свойствами.
35. Штангласы с веществами, содержащими вещества списка Б оформлены этикеткой с надписью:
а) черными буквами на белом фоне;
б) белыми буквами на черном фоне;
в) красными буквами на белом фоне;
г) белыми буквами на красном фоне;
д) красными буквами на черном фоне.
36. Красящими свойствами обладают:
б) этакридина лактат;
37. При проверке доз лекарственных веществ в лекарственных формах перорального и ректального применения учитывают, что к группе веществ списка Б отнесены:
г) экстракт белладонны;
д) натрия бензоат.
38. Кристаллизационную воду содержат:
г) магния сульфат;
39. К особо чувствительным к свету лекарственным веществам относят:
а) галеновые препараты;
в) эфирные масла;
г) серебра нитрат;
40. Защиты от воздействия влаги требуют:
а) сухие экстракты;
б) очень легко растворимые в воде вещества;
г) вещества, окисляющиеся кислородом воздуха;
д) все указанные выше.
41. Разлагаются при неправильном хранении с образованием летучих продуктов:
а) карболовая кислота;
г) натрия гидрокарбонат;
д) водорода пероксид.
42. При температуре не ниже +9 °С следует хранить:
в) ледяную уксусную кислоту.
43. С углекислым газом воздуха реагируют:
а) эфирные масла;
44. Группу пахучих веществ составляют лекарственные средства:
б) нелетучие с сильным запахом;
в) и те, и другие.
45. К группе красящих веществ относятся вещества:
а) все, имеющие окраску;
б) способные сорбироваться на таре, оборудовании, укупорочных материалах;
в) оставляющие окрашенный след, не смываемый при обычной обработке.
46. Изолированно от других видов сырья хранят растительное сырье, содержащее:
б) эфирные масла;
47. Калия перманганат взрывоопасен при контакте:
в) органическими маслами;
д) всеми перечисленными компонентами .
48. При работе с диэтиловым эфиром не допускается:
49. К взрывчатым веществам относится:
д) калия перманганат.
50. К легковоспламеняющимся веществам относятся:
а) растительные масла;
б) кислота молочная;
в) серебра нитрат;
г) перевязочный материал;
51. Нагревание огнеопасных веществ:
б) проводят при необходимости;
в) проводят на водяных банях;
г) проводят на электроплитках с закрытой спиралью.
52. Время от начала изготовления до начала стерилизации для инъекционных и инфузионных растворов не должно превышать, ч:
53. Лекарственные препараты с антибиотиками, учитывая их физико-химические и фармакологические свойства, можно изготавливать:
а) в обязательном порядке в асептических условиях;
б) изменяя значения рН в кислую или щелочную сторону;
в) вводя любые разрешенные вспомогательные вещества;
г) со стерилизацией;
д) с внутриаптечной заготовкой в виде водных растворов.
54. Сложные по составу лекарственные препараты для новорожденных, не имеющие методик качественного и количественного анализа:
а) не изготавливают;
б) изготавливают всегда «под наблюдением»;
в) изготавливают «под наблюдением» в порядке исключения.
55. Установите правильную последовательность терминов в понятии «Серия»:
а) готовый продукт;
б) определенное количество;
г) при постоянных условиях;
д) изготовленный за один производственный цикл.
56. К стерильным растворам аптечного изготовления в соответствии с НД относят растворы:
а) содержащие этанол;
б) содержащие антибиотики;
в) для новорожденных;
г) офтальмологические (для орошений);
57. Стерильные лекарственные препараты в случае нарушения целостности упаковки или укупорки повторной стерилизации:
б) не подвергают;
в) подвергают только растворы;
г) подвергают в виде исключения.
58. Розовый сигнальный цвет в виде поля на белом фоне соответствует этикетке, используемой для оформления лекарственных форм, предназначенных для применения:
в) в качестве глазных капель;
г) в качестве глазных мазей;
59. Надписи на этикетках отражают способ применения:
60. Свойства лекарственных форм как дисперсных систем отражает предупредительная надпись на основной этикетке:
а) «Беречь от детей»;
б) «Обращаться осторожно»;
г) «Перед употреблением взбалтывать»;
д) «Хранить в темном месте».
61. Контроль качества лекарственных форм и препаратов, изготовленных в аптеке, регламентирован:
а) Государственной фармакопеей;
б) Инструкцией по оценке качества лекарственных средств,
изготовляемых в аптеке;
в) Приказом Минздрава России «О контроле качества лекарственных средств, изготовляемых в аптеках»;
г) ОСТ 91500.05.001–00 «Стандарты качества лекарственных средств. Основные положения»;
д) всеми указанными НД.
62. После изготовления препарата паспорт письменного контроля хранят в аптеке:
63. Формулы, используемые при расчетах, в паспорте письменного контроля (ППК):
в) указывают, если они включены в общие фармакопейные статьи.
Вам что-то еще надо? воспользуйтесь поиском по сайту: